地球も含め地上の物質はすべて様々な元素が集まって形作られている。例えば、地球は鉄35%、酸素28%、マグネシウム17%、ケイ素13%、硫黄やカルシウム等々が集まって地球を形成し、酸素65%、炭素18%、水素10%等々が集まって人体は存在しています。現在まで見つかっている元素は118種類で酸素もその元素のひとつです。
中でも酸素は身近すぎて気付かれませんが、非常に特殊な性質を持っている元素です。私たちが生きるために不可欠な酸素は酸素原子O(電子8個)が2つ結合した酸素分子(電子16個)O2ですが実態は激しい性格で強い毒性を持っています。
しかし、この特殊な性質や毒性を上手に使い分けて生きていることも事実です。酸素を知ることは体内で起こっている膨大な化学反応を知る上で絶好の分子です。
酸素の特殊な性格は電子にあり
- 【目次】
- 電子
- 酸素はフリーラジカル
- 酸素の毒性
- 姿を変える酸素
電子
さて、酸素の特殊な性格は「電子」の数と配置によるものですので原子構造を簡単におさらいする必要があります。苦手意識を持つ方が多い世界ですので基本だけを簡単に説明しますが、原子や分子は陽子と電子(中性子は省略します)で構成されています。原則、電子は夫婦ペア(2個)で安定し、一人ぼっちだと不安定な性格となります。下記図は安定状態の水素と不安定な状態酸素(三重項酸素)の電子配置を比べたものです(左が水素分子、右が酸素分子)。
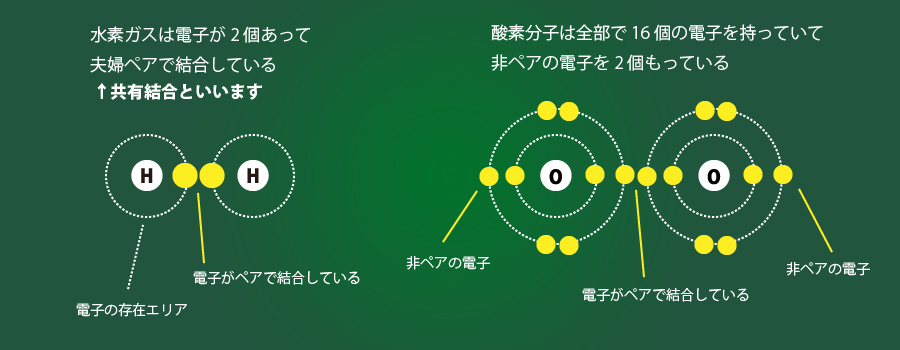
酸素はフリーラジカル
混乱を避けるため陽子などは省略していますが、酸素のように非ペアの電子のことを不対電子といい、不対電子を持つ原子や分子をフリーラジカルと呼びます。ついでに、フリーラジカルは独身の電子を結婚させるために働く宿命を持っているためどうしても不安定になります。
そして、酸素の特殊な性質は、図で見ると両端の電子がペアにならずに比較的安定した状態で存在できるところにあります。※酸素は二個の不対電子を持つためビラジカルと呼びます。また、世の中の物質の大半は不対電子をもっていませんので、これだけでも酸素の特殊性がわかるというものですね。
酸素の毒性
地球上の多くの生物は、進化の過程で酸素を使って効率よくエネルギーを生産できるようシステムを構築してきました。余談ですが酵母は酸素を利用できますが、酪酸菌は酸素を利用するものならその毒性で直ちに死んでしまう。この違いは、酸素の毒性を無毒化できるか否かの違いによるものです。
乳酸菌は酸素を利用してエネルギーをつくることは出来ないが、毒性を無毒化することが出来るので周りに酸素があっても生き延びられるんです。酸素の毒性がいかに侮れないものかわかっていただけたでしょうか。。
姿を変える酸素
では、普段気にせず吸い込んでいる酸素の毒性はいつ発揮されるのでしょうか。簡単に結論付けると姿を変えるときにその毒性が発揮されます。ここで、体内で発生する主な酸素種をまとめると
- 三重項酸素(空気中にある普通の酸素の正式名称)
- 一重項酸素
- スーパーオキシド・ラジカル
- 過酸化水素
- ヒドロキシル・ラジカル
となります。1は普通の酸素なので4種類あることになります。また、毒性もそれぞれ違っていて「活性酸素」と呼ばれることもあります。
次のページへつづく>>>>



